Chapitre 3 : Les changements d'états en cuisine
Chapitre 3. Les changements d'état en cuisine
I. Quels sont les différents changements d'état qui existent et comment les interpréter ?
Activité 1. Les changements d'état de l'eau
![]() 5° chap 3 AFE1 les changements d etats
5° chap 3 AFE1 les changements d etats
AFE1 les changements d'états correction. ![]()
A RETENIR :
Fusion : passage de l’état solide à l’état liquide.
Liquéfaction : passage de l’état gazeux à l’état liquide.
Solidification : passage de l’état liquide à l’état solide.
Vaporisation : passage de l’état liquide à l’état gazeux.
Dans les conditions normales, l’eau liquide pure devient solide à 0°C.
L’eau liquide passe sous forme de vapeur d’eau à 100°C.
Activité 2. Que se passe-t-il à l'échelle microscopique lors d'un changement d'état ?
![]() 5° chap 3 AFE2 interpretation microscopique
5° chap 3 AFE2 interpretation microscopique
AFE2 interprétation microscopique correction ![]()
A RETENIR :
Lors d’un changement d’état, l’agitation des molécules est modifiée jusqu’à ce que les liaisons entre les molécules se cassent ou se créent.
Lors de la vaporisation, les liaisons se cassent et on passe d’un état compact désordonné à un état dispersé désordonné.
Lors de la solidification, les molécules arrêtent de bouger les unes par rapport aux autres, les liaisons se figent, on passe d’un état compact désordonné à un état compact ordonné.
II. Comment évoluent la masse et le volume au cours des changements d'états ?
Activité 3. Pêché de gourmandise ?
AFE3 masse et volume correction.pdf ![]()
A RETENIR :
Lors d’un changement d’état, la masse se conserve car le nombre de particules ne change pas.
Lors d’un changement d’état, le volume ne se conserve pas.
Exemple : au cours de la solidification de l'eau pure, le volume augmente et au cours de la fusion, il diminue.
III. Comment évolue la température au cours d'un changement d'état ?
A RETENIR :
Une température se mesure grâce à un thermomètre. Le symbole de la température est T. L’unité de la température est le degré Celsius °C.
Regardez la vidéo suivante pour voir toutes les étapes pour construire un graphique :
Fiche méthode graphique correction.pdf ![]()
Activité 4. Du verre d'eau liquide au glaçon
![]() 5° chap 3 AFE4 du verre d eau au glaçon
5° chap 3 AFE4 du verre d eau au glaçon
AFE4 du verre d'eau au glacon correction ![]()
A RETENIR :
L’augmentation de la température d’un corps pur nécessite l’apport d’énergie.
Les changements d’états d’un corps pur mettent en jeu des transferts d’énergie.
Un palier de température apparaît lors du changement d’état d’un corps pur.
La température de changement d’état de l’eau correspond à la température à laquelle se produit le changement d’état. Cette température correspond à celle du palier.
Exemple : dans les conditions normales, la température de solidification de l’eau pure est 0°C.
Activité 5. De l'eau bouillante pour faire cuire les pâtes
AFE5 De l'eau bouillante pour faire cuire les pates ![]()
A RETENIR :
Dans les conditions normales, la température de vaporisation de l’eau pure est de 100°C.
Pour aller plus loin... peut-on faire bouillir de l'eau à une température inférieure à 100 °C ?
Dans "les conditions normales" signifie que l'on se place pour faire les expériences dans un environnement où la pression de l'air est égale à la pression atmosphérique, c'est-à-dire la valeur de la pression de l'air au niveau de la mer ou dans la salle de classe. La pression est une grandeur physique qui est reliée à la quantité d'air qui est présente au lieu où l'on se situe. Plus la quantité d'air est grande, plus la pression de l'air est grande. A l'inverse, moins il y a d'air, et plus la pression est faible.
Tout cela pour dire qu'il est possible, si la pression est suffisamment faible, de faire bouillir de l'eau à une température inférieure à 100°C.
Pour s'entraîner
EXERCICES :
![]() Exercices chap3 5e (277.26 Ko)
Exercices chap3 5e (277.26 Ko)
exercices chap3 correction.pdf ![]()
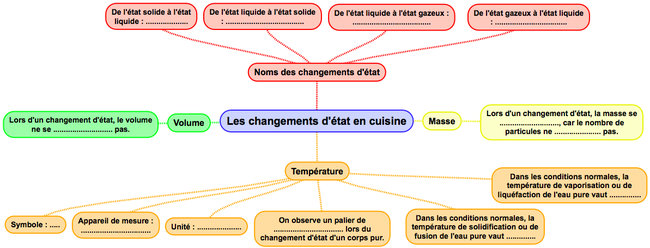
CARTE MENTALE :
EVALUATION BLANCHE :
Faire ensuite l'évaluation blanche, puis corriger vos erreurs à l'aide de la correction.
Evaluation blanche n°2
Correction de l'évaluation blanche n°2